2.1. Уравнение состояния идеального газа
Уравнение состояния термодинамической системы представляет собой аналитическую формулу, связывающую параметры состояния системы. Если состояние системы может быть полностью описано с помощью трех параметров: давления 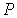 , объема 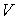 и температуры 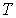 , то уравнение состояния в самом общем виде будет иметь форму:
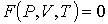 . . | (2.1) |
Конкретный вид этой формулы зависит от физических свойств рассматриваемой термодинамической системы.
Обобщение многочисленных экспериментальных данных показывает, что большинство газов при комнатной температуре и давлении порядка одной атмосферы (при нормальных условиях) с достаточно высокой точностью могут быть описаны уравнением состояния, называемым уравнением Клапейрона-Менделеева:
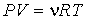 , , | (2.2) |
В рамках термодинамического подхода газ, уравнение состояния которого, связывающие параметры 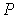 , 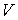 , и 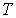 , является уравнением Клапейрона-Менделеева (2.2), называется идеальным газом. При нормальных условиях наиболее близкими по своим свойствам к идеальному газу являются водород и гелий.
Подробный анализ уравнения (2.2) начнем с обсуждения величины 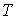 , которая называется абсолютной температурой. Из формулы (2.2) следует, что при постоянном объеме и количестве вещества температура 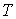 пропорциональна давлению идеального газа 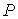 . А это означает, что если измерение температуры проводить с помощью газового термометра постоянного объема, в качестве рабочего тела в котором используется идеальный газ, то такой термометр будет иметь линейную шкалу температур. Очевидно, что использование газового термометра для определения абсолютной температуры ограничено, так как в качестве термометрического тела может быть использован только реальный газ, свойства которого отличны от идеального, и для которого уравнение (2.2) является приближенным. При низких температурах реальный газ переходит в жидкое состояние, что делает невозможным его использование при этих температурах в качестве рабочего тела газового термометра.
Абсолютная температура 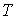 , измеренная с помощью рассмотренного идеально-газового термометра, связана с температурой, определенной по шкале Цельсия, выражением:
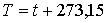 , , | (2.3) |
где 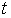 - численное значение температуры по шкале Цельсия. Единицей измерения температуры 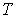 в абсолютной шкале температур является кельвин (К), численно совпадающий с единицей измерения температуры по шкале Цельсия - градусом Цельсия ( oС).
В соответствии с формулой (2.2) при абсолютной температуре 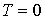 К произведение 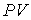 обращается в ноль. Это значение температуры называется абсолютным нулем температуры. Так же как и произведение давления на объем 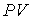 , абсолютная температура не может иметь отрицательных значений. Из (2.3) следует, что абсолютному нулю температуры соответствует  o oC.
Перейдем к обсуждению введенного в формуле (2.2) параметра 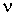 , который характеризует количество вещества, в данном случае идеального газа. С молекулярно-кинетической точки зрения, эта величина пропорциональна количеству молекул, входящих в систему. Очевидно, что от количества молекул в системе будут зависеть ее термодинамические свойства. Поэтому 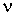 также как 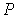 , 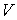 , и 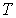 является термодинамическим параметром системы и уравнение состояния (2.2) связывает все эти четыре термодинамических параметра. Так как термодинамика не рассматривает молекулярную структуру вещества, то в ее рамках количество вещества может быть определено только из термодинамических соотношений на основе экспериментальных данных.
Проведенные опыты показали, что соотношение между параметрами 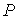 , 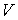 , и 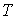 для разных газов остается одинаковым, если между их массами поддерживается определенное постоянное соотношение. Например, коэффициент пропорциональности между произведением давления газа на его объем: 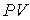 , и температурой 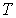 остается одинаковым как для 2 грамм водорода, так и для 32 грамм кислорода. Из этого следует (см. формулу (2.2)), что количество вещества 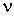 можно определить как отношение массы 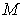 газа к некоторой постоянной для данного газа величине 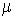 :
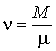 , , | (2.4) |
Понятие количества вещества исторически было сначала введено в химии для определения соотношения между массами вступающих в реакцию и получаемых в ней химических веществ. Это наложило отпечаток на определение единицы измерения количества вещества. Количество вещества измеряется в молях. Эта единица измерения внесена в список основных единиц системы СИ.
Количество молекул в одном моле любого вещества одинаково и численно равно постоянной Авогадро, названной в честь итальянского физика и химика Амедео Авогадро (1776 - 1856). Величина этой постоянной определялась экспериментально и численно равна:
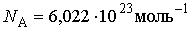 . . | (2.5) |
Постоянная Авогадро показывает соотношение масштабов масс в макро- и микромире и является единицей измерения числа частиц в термодинамической системе. Она позволяет ввести критерий применимости термодинамического подхода при описании систем. Если число частиц в системе сравнимо или значительно превышает постоянную Авогадро, то для такой системы возможно термодинамическое описание.
Постоянная Авогадро связана с величиной, называемой атомной единицей массы (а.е.м.). Эта величина численно равна одной двенадцатой массы изотопа углерода 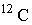 :
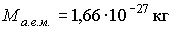 . . | (2.6) |
Отношение одного грамма (10 -3 кг) к атомной единице массы дает значение постоянной Авогадро.
Массу одного атома 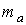 можно определить как произведение атомной единицы массы 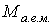 на атомную массу элемента 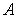 , указанную в таблице Менделеева:
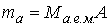 . . | (2.7) |
Масса одной молекулы 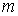 определяется как сумма масс атомов, входящих в неё. Умножение получившегося выражения на постоянную Авогадро дает молярную массу вещества:
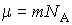 . . | (2.8) |
Молярная масса измеряется в кг/моль.
В уравнении Клапейрона-Менделеева (2.2) в качестве коэффициента пропорциональности между величинами 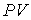 и 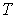 стоит произведение количества вещества 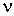 на коэффициент 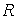 , который называется универсальной газовой постоянной. Эта одинаковая для всех газов величина равна:
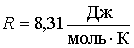 . . | (2.9) |
Подстановка выражения для количества вещества (2.4) в уравнение Клапейрона-Менделеева (2.2) приводит его к окончательному виду
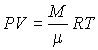 . . | (2.10) |
Уравнение Клапейрона-Менделеева описывает равновесные состояния идеального газа, а, следовательно, и любые обратимые процессы, которые в нем могут протекать. При наложении на систему дополнительных условий, можно получить уравнения термодинамических процессов, и соответствующие им законы, которые имеют ограниченное применение и являются частными случаями допускаемых уравнением (2.2) термодинамических процессов.
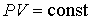 . . | (2.11) |
Указанная связь между давлением и объёмом была независимо друг от друга изучена во второй половине ХVII века английским физиком Робертом Бойлем (1627 - 1691) и французским физиком Эдмом Мариоттом (1620 - 1684). В шестидесятых годах ХVII столетия Бойлем были проведены опыты по определению изменения объёма, занимаемого постоянным количеством воздуха, в зависимости от давления. Эти опыты носили чисто прикладной характер, связанный с разработкой и усовершенствованием Бойлем воздушных насосов. Для своих опытов Бойль использовал стеклянные трубки, запаянные с одного конца, в которые он заливал ртуть, оставляя около запаянного конца пузырёк воздуха. При измерениях для давления выше атмосферного использовалась изогнутая V-образная трубка, а в случае давления ниже атмосферного - прямая трубка, открытый конец которой помещался в сосуд с ртутью. По объёму пузырька и высоте столба ртути Бойль рассчитывал соотношение между давлением и объёмом воздуха. Полученные им данные подтвердили обратную зависимость между давлением и объёмом воздуха. В 1676 году закон Бойля был заново открыт Мариоттом, который рассматривал его как одно из фундаментальных свойств газов.
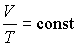 , , | (2.12) |
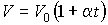 , , | (2.13) |
где: 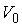 - объем газа при температуре равной нулю градусов по шкале Цельсия, 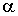 - температурный коэффициент расширения газа, который для идеального газа должен быть равен 1/273,15. Для реальных газов при нормальных условиях он близок к этому значению.
Если оставлять неизменным объем газа, что, например, имеет место в газовых термометрах постоянного объема, то происходящий при этом процесс будет называться изохорическим ( 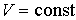 ) и описываться уравнением:
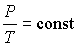 . . | (2.14) |
Процессы в идеальном газе, происходящие при постоянстве одного из параметров состояния: температуры, давления или объема (см. уравнения (2.11), (2.12) и (2.14)), называются изопроцессами. Протекание этих процессов ограничено дополнительными внешними воздействиями, делающими один из параметров состояния постоянным. По этой причине эти процессы необходимо рассматривать только как частные случаи, которыми не ограничен перечень всех возможных обратимых процессов в идеальном газе.
|